双抗市场即将爆发?武田与F-star 就新型下一代免疫肿瘤双特异性抗体签订许可协议
文章来源:凯莱英药闻
2022年7月20日,F-star Therapeutics(简称“F-star”)宣布已与武田签订许可协议。根据协议条款,F-star将授予武田使用 F-star 专有的 Fcab 和 mAb 2 平台,针对免疫肿瘤靶点的双特异性抗体进行研究、开发和商业化的全球独家特许权使用许可。武田将负责协议项下的所有研究、开发和商业化活动。F-star 将获得 100 万美元的预付款;倘若实现所有里程碑,F-star 将有资格获得高达约 4000 万美元的开发和商业化里程碑付款,以及年净销售额的特许权使用费。

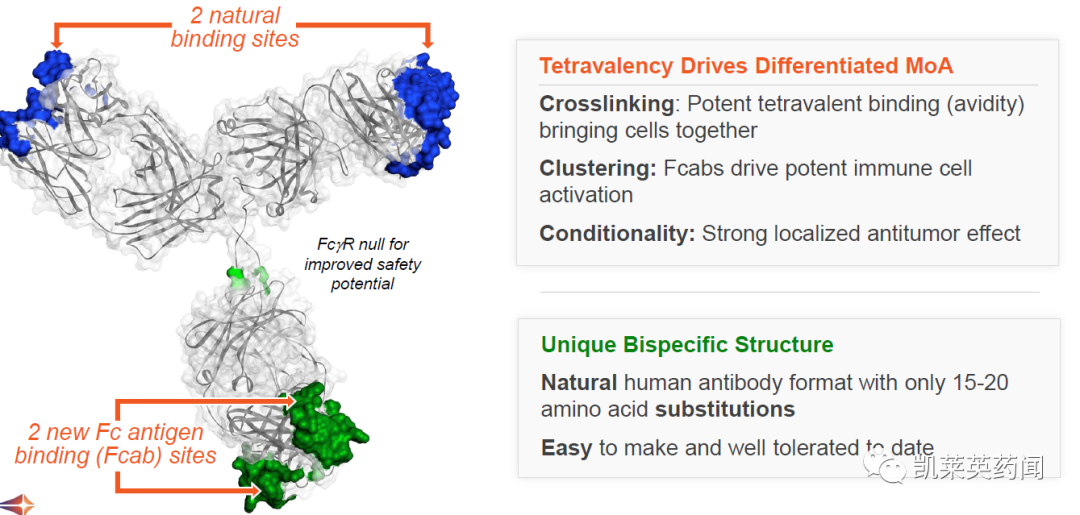
F-star是一家临床阶段生物制药公司,致力于开发下一代免疫疗法以改变癌症患者的生活。公司致力于通过使用四价 (2+2) 双特异性抗体来实现治疗的范式转变,从而实现无癌症和其他严重疾病的未来。其中,mAb 2 是一个对称性设计的、具有Fc全长的、4个结合表位的双特异性抗体平台。它的优点是:1)由于获得的双抗结构对称,与天然IgG近似,因此在成药性及CMC方面有一定优势;2)筛选到抗体Fc的CH3部分的分子(Fcab)具有高亲和力,可以与任何Fab进行组装形成双抗,从而提高研发效率。
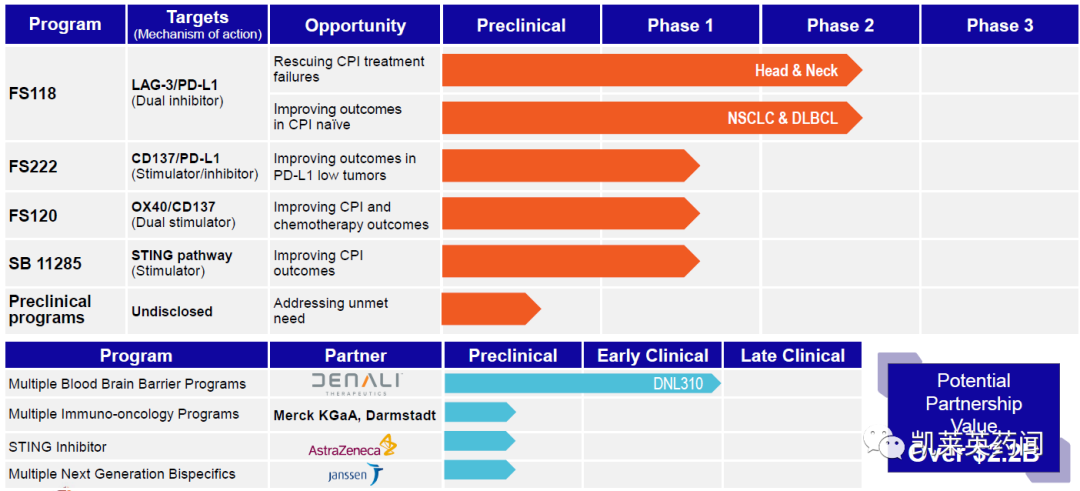
目前,F-star有 4个项目进入临床,还有多个未公开的项目正在开发中。近年来,F-star与多家跨国巨头,包括默克、阿斯利康、强生等,在肿瘤、免疫及神经系统等一系列治疗领域展开合作。2022年6月,中国生物子公司 invoX Pharma(简称“invoX”)拟以总价1.61亿美元(约10.8亿人民币)或每股7.12美元的价格,收购F-star;本次交易中,中国生物可以获得F-star旗下包括FS118、FS222、FS120在内的多款双抗药物。消息公布后,F-star 的股票在周四早盘交易中上涨了 65%,接近收购价。
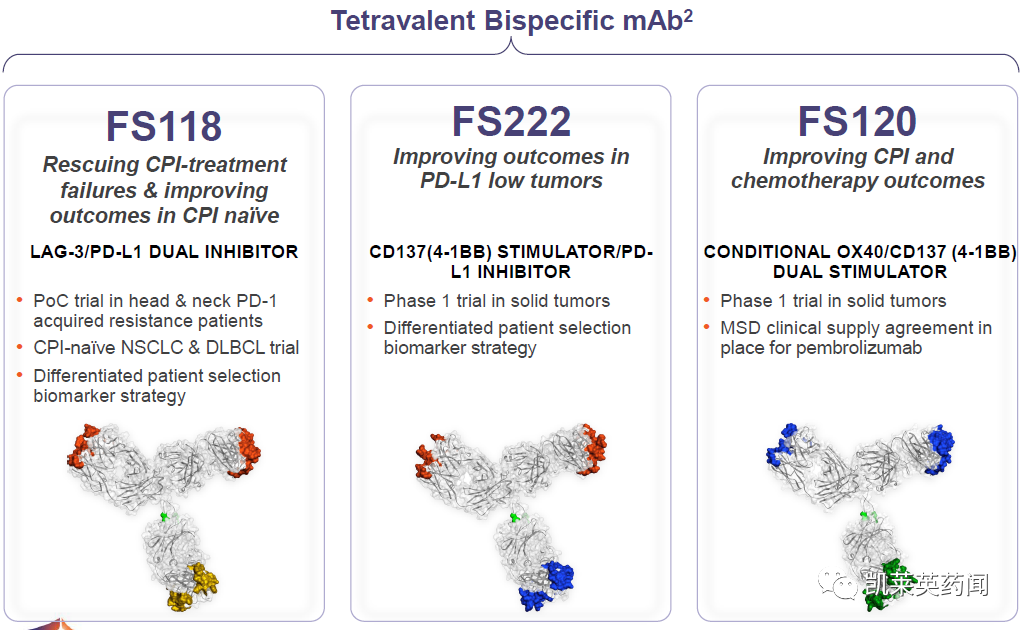
其中,FS118是一种靶向PD-L1及LAG-3的双检查点抑制剂,目前正在进行对检查点抑制剂具有获得性耐药的头颈部癌症患者的2期临床试验以及检查点抑制剂初治的非小细胞肺癌(NSCLC)及弥漫性大B细胞淋巴瘤(DLBCL)患者的临床试验。FS222,一种双重靶向CD137(4-1BB)激动剂及PD-L1抑制剂;FS120,一种靶向OX40及CD137(4-1BB)的双重激动剂。
invoX于 2021 年在英国成立,是中国生物的国际扩张平台,专注于中国以外的研发和业务发展活动,核心专注于肿瘤和呼吸领域。此前,公司已收购了另外两家生物技术公司,即Softhale和 pHion Therapeutics的多数股权。F-star 将成为 invoX 战略的关键要素,加速中国生物制药开发创新药物,改变全球患者的生活,补充其现有的研发平台和管线。
双体可以同时结合2个不同的靶点,其中一边直接与癌细胞上的特定抗原结合,另一边则激活患者自身免疫系统中的T细胞并使其更接近癌细胞将它杀死。由于具备功能上的改进,双抗相比单抗,有更复杂的结构。它的临床价值在于:
1)对比两个单抗联用,潜在的安全性优化、疗效优化,以及技术成熟后的费用下降。
2)通过新功能——桥接,可以直接招募免疫细胞,起到更强的杀伤作用。待开发的还有穿越血脑屏障的功能。
3)通过新功能——和一个细胞上的2个靶点结合,可以起到双重信号阻断的作用,防止旁路信号的激活。
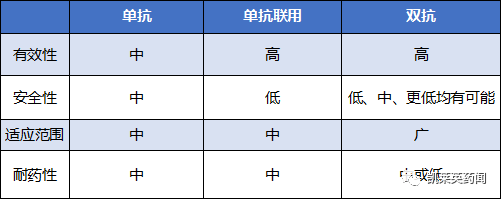
双抗对比其他抗体药物差异
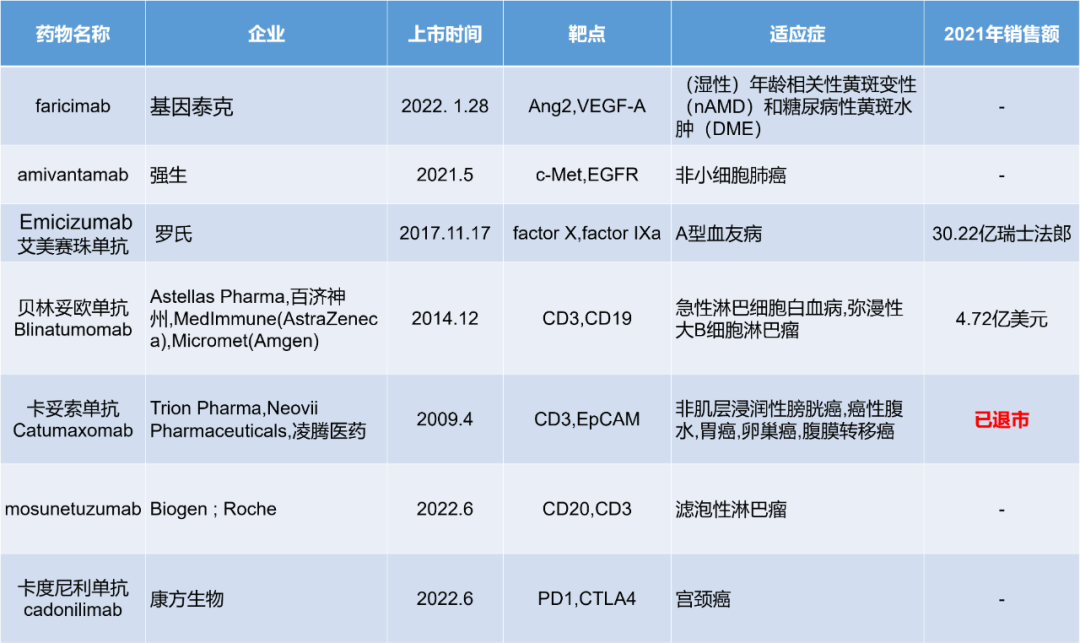
目前,全球已有7个双抗获批上市,具体信息统计如下:
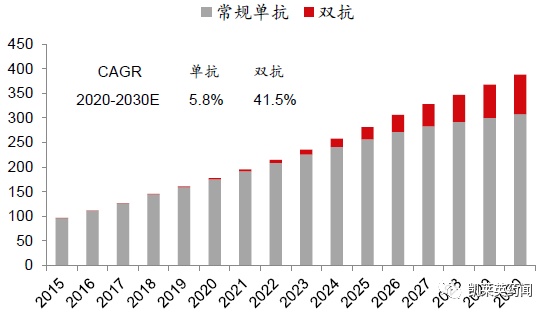
根据弗罗斯特沙利文的数据,2020年全球的单抗规模1749亿美元,预计2024-2030年行业增速4.2%。2020年双抗行业市场规模25亿美元,2024-2030年行业增速预计29.3%。双抗行业增速高于单抗。
全球双抗/单抗药物市场规模和增速
(单位:十亿美元)
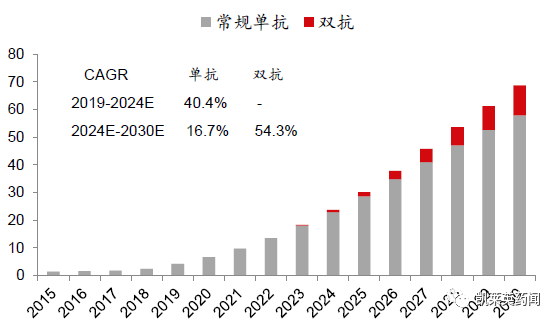
预计2030年中国的双抗市场达到108亿美元,2024-2030年增速54.3%;单抗市场规模579亿美元,2024-2030年增速16.7%。双抗行业增速高于单抗。
中国的双抗/单抗药物市场规模和增速
(单位:十亿美元)
-
2022-09-15
39个国家级核酸药物技术攻关项目立项,不
国家生物药技术创新中心发布2022年国家生物药技术创新中心核
-
2022-08-17
本周创新药NDA和IND汇总
文章来源:凯莱英药闻「收集周期:8月8日-8月13日,包括“
-
2022-08-04
2022年7月国内生物医药投融资汇总
文章来源:凯莱英药闻2022年7月,我国有25家创新药企完成
-
2022-07-22
双抗市场即将爆发?武田与F-star 就
文章来源:凯莱英药闻2022年7月20日,F-star Th…
-
2022-07-14
【药政】2022年6月医药行业政策
文章来源:微信公众号6月,NMPA发布《2021年度药品审评
